Oltingugurt

S vulqon jinsi sifatida eramizdan ilgari II asrda ma’lum bo’lgan. Toza oltingugurt oddiy sharoitda mo’rt kristall, sariq rangli modda suvda erimaydi, ayrim organik erituvchilarda eriydi. 1130C da suyuqlanadi, zichligi 2, 07g/sm3 4460 C da qaynaydi. U tipik metallmas kimyoviy reaksiyalarga oson kirishadi. Metallar bilan sulfidlar hosil qiladi, galogenlar, kislorod, vodorod bilan oson birikadi. Tabiatda keng tarqalgan yer qobig’ining 0,1 % tashkil etadi. U ham erkin holda ham birikmalar shaklida uchraydi. Tug’ma oltingugurtning yirik konlari turkmaniston (Qoraqum), O’zbekiston (Farg’ona) va Volga bo’ylarida joylashgan. AQSH, Italiya va Yaponiyada yirik konlari bor.
Tug’ma oltingugurt tarkibida oltingugurtning massa ulushi 30 % dan oshmaydi. Undan begona aralashmalarini (qum, tuproq, ohaktosh va boshqalar) ajratish uchun, ruda yaxshilab maydalanadi kerosin qo’shib flotasiyalanadi. Olingan konsentrat tarkibida 80% gacha S saqlaydi. So’ngra konsentrat avtoklovda (yuqori bosimda ishlovchi apparatga avtoklov deyiladi) 600 kPa bosim ostida bug’ bilan (140-1500C) suyuqlantirilib toza oltingugurt ajratib olinadi. Shunday yo’l bilan tozalab olingani oltingugurt deyilib 98-99% li bo’ladi. Oltingugurt yana pirit FeS2 palaxsa-palaxsa va mis rudalarini suyuqlatirish orqali olinadi. Masalan: piritni 6000C ga maxsus pechlarda ozroq mayda koks qo’shib qizdirish orqali olinadi.
FeS2 S + FeS
FeS oksidlanib hosil bo’lgan SO2 uglerod bilan qaytarilib S ga aylanadi. Ba’zi chet mamlakatlarda (masalan AQSH da) yer ostida S ni suyuqlantirib olish usullari ham tarqalgan S olishning keyingi keng tarqalgan usullaridan yana biri bu vodorod sulfidni chala oksidlab olish usulidir.
Ko’mirni gazga aylantirganda hosil bo’lgan mahsulotlarni (suv, havo va yoritgich gazlari) desulfurlash orqali S ajratib olinadi. Masalan: havo va katalizator aktiv ko’mir ta’sir etib olinadi. Har ikkala holda ham quyidagicha reaksiya boradi.
2H2S + O2 = 2S + 2H2O
Natriy tiosulfat eritmasiga kislotalar ta’sir etib olinadi. (bu reaksiya laboratoriyada reaksiya tezligi mavzusida o’tiladi)
Na2S2O3 + 2HCl = 2NaCl + SЇ +H2O + SO2
Ba’zan, oltingugurt, tarkibida oltingugurt bo’lgan gazlardan ham olinadi. Masalan, H2S dan oltingugurt olish uchun texnikada quyidagi reaksiyalardan foydalaniladi.
2H2S + 3O2 = 2SO2 + 2H2O 2H2S + SO2 = 3S + 2H2O
Oltingugurtning kristall holatdagi allotropik modifikasiyalaridan eng muhimi ikkita: rombik yoki oktaedrik oltingugurt (a-oltingugurt) va monoklinik yoki prizmatik oltingugurt (β-oltingugurt).

Tabiatda uchraydigan rombik oltingugurtning solishtirma og’irligi 2,07 suyuqlanish harorati 112,8oC. Rombik oltingugurt 95,5oC dan past haroratlardagina barqaror bo’ladi, 95,5°C dan yuqorida monoklinik oltingugurt barqarordir. Monoklinik oltingugurt prizma shaklidagi tinik kristallardan iborat bo’lib, uning solishtirma og’irligi 1,96g/sm3, suyuqlanish harorati 119,3°C. Rombik oltingugurtni, masalan, 100°C da uzoq vaqt tutib turilsa, u monoklinik oltingugurtga aylanadi. 95,5°C da monoklinik oltingugurt bilan rombik oltingugurt muvozanat holatida bo’ladi:
S rombik = S monoklinik
Bu harorat rombik va monoklinik oltingugurtlarning bir-biriga aylanish haroratidir.
Odatdagi sharoitda, qattiq oltingugurt molekulasi halka tarzida bir-biri bilan tutashadigan 8 atomdan tarkib topadi; S8 qizdirilganda S8 halkasi uziladi. Yuqori haroratda zanjir bo’laklari mavjud bo’ladi. 448oC da oltingugurt qaynaydi. Bug’ holatda oltingugurt molekulalari S8, S6, S4 va S2 orasida muvozanat qaror topadi (harorat qanday bo’lishiga qarab).
Oltingugurt erkin holda turli son molekulalaridan iborat bo’lib, (SҐ, S12, S8, S6, S2) halqali tuzilishga ega. Bu molekulalar turlicha tartibda o’zaro bog’lanishi mumkin. Shuning uchun oltingugurt bir necha allotropik shakl o’zgarishlarda uchraydi. Uy haroratida a- oltingugurt shaklida (rombik) sariq, mo’rt kristall, 960C dan yuqori haroratda a-S sekinlik bilan b-S ga aylanadi. (suyultirib sekin sovutilsa a-S, b-S ga aylanadi.) (monoklinik oltingugurt) oq rangli kristall plastinkalardan iborat. (a-S ts= 1130C, b-S ts= 1190C)
Suyuqlantirilganda suyuq sariq rangli S8 formulaga javob beruvchi zanjir tuzilishli oltingugurt hosil bo’ladi.

Yanada qizdirilsa (2500C ga cha) yopishqoq oquvchanligini qarib yo’qotgan oltingugurt hosil bo’ladi, u qizil – qo’ng’ir rangli yopishqoq suyuqlikdir. Oltingugurtni undan yuqori haroratda (3000C dan yuqorida) qizdirilsa qo’ng’ir rangli oquvchan suyuqlikka aylanadi. Bu suyuqlikni tez sovutilsa (suvga solinsa) sariq-qo’ng’ir rangli plastik oltingugurtga aylanadi, uni pichoq bilan kesish mumkin, rezinaga o’xshashli chuziluvchan bo’lib, havoda bir necha minut turgach yana rombik oltingugurtga aylanadi.
Oltingugurtning reaksion qobilyati odatdagi haroratda u qadar yuqori emas; uning havoda alangalanish harorati 120°C ga yaqin. Uy haroratida u ishqoriy metallar bilan, mis, kumush va simob bilan reaksiyaga kirishishi uchun uni suyuqlanish haroratiga qadar qizdirish kerak.
Vodorod bilan oltingugurt birikishi uchun ancha yuqori harorat talab qilinadi.
2Na + S = Na2S 2K + S = K2S
Cu + S = CuS 2Ag + S = Ag2S
Hg + S = HgS 2S + CI2 = S2CL2
H2 + S = H2S
Oltingugurt ishqorlar bilan qizdirilganda quyidagi reaksiya boradi.
3S + 6NaOH → 2Na2S + Na2SO3 + 3H2O
Oltingugurt keng sohalarida ishlatiladi. Dunyoda ishlab chiqariladigan oltingugurtning 50% dan ko’progi sulfat kislota ishlab chiqarish uchun ishlatiladi. Ko’p miqdorda rezina sanoatida kauchukni vulkanlashda, o’simlik zararkunandalariga qarshi kurashda, gugurt ishlab chiqarishda, bo’yoq olishda (ko’k bo’yoq), CS2 olishda, teri kasalliklarini davolashda, turli dori-darmonlar olisha, qora porox tayyorlashda, Ca(HSO3)2 olishda va boshqa sohalarda ishlatiladi.
5, 10, 20 % li oltingugurt teri kasalliklarida (psoriaz, qichima) surtma va sepma dorilar holatida qo’llaniladi.

- A.E.Fersman oltingugurtni «kimyo sanoatining dvigateli» deb atagan.
- Tibbiyot maqsadlari uchun ishlatiladigan S quyidagicha olinadi:
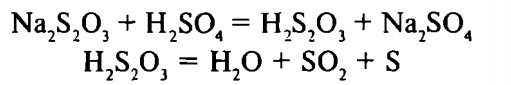
Vodorod sulfid
Tabiatda keng tarqalgan tabiiy gaz tarkibida uchraydi, oqsil moddalarini parchalanishidan hosil bo’lib turadi, yer osti suvlarida bo’ladi, juda zaharli modda 0,08% ( hajmda) H2S ni 5-10 minut hidlab turilsa odamni o’ldiradi. H2S xuddi HCN ga o’xshab nafas olish fermentini (sitoxromni) bog’lab olib yaroqsiz holga keltiradi. Laboratoriyada u bilan ishlaganda mo’rili shkafda ishlash ehtiyot bo’lish zarur. Uni qo’rg’oshinli qog’ozni (Pb-ning (II)- valentli tuzlarni suvdagi eritmasiga filtr qog’ozini ho’llab quritilgani) qora-qo’ng’ir rangga bo’yashidan bilib olish mumkin. Kumush metali qorayadi. ( Ag2S hosil bo’ladi) va hokazo.
Olinishi: Sanoatda: 1) H2S suv gazini tabiiy gazni, koks gazi, hamda sintez gazlarini aminokislotaning natriyli tuzlari bilan yoki etanolamin bilan tozalanganda ushlab qolingan H2S ajratib olinadi. 2) FeS va HCl bilan ishlov berib olinadi. FeS+2HCl=FeCl2+H2S
3) S- ni parafin bilan qizdirib olinadi.
4) S va H2 dan tog’ridan-tog’ri sintezlash orqali olinadi. Keyingi 3 ta usul lobaratoriya usulidir.
Rangsiz hidlangan tuxum hidiga ega -610 C da qaynaydi, yonadi (havorang alanga bilan) 2H2S+3O2=2H2O+2SO2
Suvda kam eriydi, chala yonsa S va suv hosil qiladi.
2H2S+O2=2S+2H2O
Vodorod sulfid, tabiatda ba’zi shifobaxsh mineral suv manbalarida va oz miqdorda vulkon gazlar tarkibida uchraydi. Yuqori haroratda H2 bilan S ni biriktirib ham H2S ni sintez qilinadi.
H2 + S = H2S
Laboratoriyada H2S olish uchun metallarning sulfidlariga xlorid
kislota yoki sulfat kislotaning suyultirilgan eritmalari ta’sir ettiriladi.
FeS + 2HCL = FeCL2 + H2S
Vodorod sulfid-rangsiz juda zaharli gaz. Uning muzlash harorati -83.6°C. H2S gazi -60.75°C da suyuqlikka o’tadi. Suyuq holatdagi H2S amalda elektr tokini o’tkazmaydi. Qattiq qizdirilganda H2S vodorod va oltingugurtga ajraladi. H2S=H2+S. H2S havoda yonadi:
2H2S+3O2=2SO2+2H2O
Agar havoda yonib turgan H2S alangasi sovuq sirtga tutilsa yonish natijasida hosil bo’layotgan oltingugurt idish devoriga utiradi.
2H2S + O2 = 2S + 2H2O
H2S suvda eritilganda kuchsiz sulfid kislota hosil bo’ladi. (1l suvda 0°C da 4,6 l H2S, 20°C da esa 2,6 l H2S eriydi). Sulfid kislota ikki negizli kislotadir.


Vodorod sulfid asos va tuzlarning eritmalariga yuborilganida metall sulfidlari hosil bo’ladi. Suvda erimaydigan sulfidlar tegishli tuzlarning eritmalaridan H2S o’tkazish yo’li bilan cho’kma holida hosil qilinadi. Kaliy gidroksid eritmasi H2S bilan to’yintirilganda avval kaliy gidrosulfid hosil bo’ladi:
KOH + H2S = KHS + H2O
Eritmaga yana ishqor qo’shilganda (ya’ni mo’l ishqor bo’lganda) kaliy sulfid hosil bo’ladi.
KHS + KOH = K2S + H2O
Natriy sulfid natriy sulfatni ko’mir yordamida qaytarish yo’li bilan olinadi.
Na2SO4 + 4S = Na2S + 4CO
Ammoniy gidroksid eritmasiga H2S yuborish orqali ammoniy gidrosulfid NH4HS hosil qilinadi. Bu modda hatto 0°C da va 350 mm sim.ust. bosimidayoq quyidagicha parchalanadi.
NH4HS <==> NH3 + H2S
Kristallik ammoniy sulfid (NH3)2Sfaqat past haroratlardagina hosil qilina oladi. Laboratoriyalarda qo’llaniladigan ammoniy sulfid eritmasi NH4HS va NH3 ning ekvimolekulyar aralashmalaridan iborat.
Ishqoriy va ishqoriy yer metallar sulfidlarining suvdagi aralashmalari beqaror bo’ladi. Chunki bu sulfidlar havoda osonlik bilan oltingugurtga qadar oksidlanadi. Hosil bo’lgan oltingugurt osongina metall sulfid eritmasida erib polisulfidlarni beradi. Masalan, Na2S eritmasidan Na2S3.8H2O tarkibli natriy polisulfid hosil bo’ladi:
Na2S + 2S = Na2S3
Og’ir metallarning sulfidlari, masalan; HgS, PbS, Sb2S3, CuS, CdS, ZnS, MnS, NiS o’zlariga xos rangga ega bo’lib, suvda yomon eriydi.
Ana shu sababli kationlarni bir-biridan ajratishda bunday sulfidlar hosil bo’lishidan foydalaniladi, chunki ularning ba’zilari suyultirilgan HCl eritmasida eriydi, ba’zilari suvda ham, HCl ning suyultirilgan eritmasida ham erimaydi.
- SO2 nam havoda chang bilan tumansimon g’ubor hosil qilib muallaq holatda sulfat kislota tomchisiga aylanadi va bahorgi yog’inda o’simlik ustiga “kislotali yomg’ir bo’lib tushadi.”
- S2O3-oltingugurt yarim oksidi.Suvsiz SO3 ga S ta’sir ettirib mayda ko’kimtir qirindi krsital holda olinadi: SO3+S=S2O3
S2O3-suvda kam eriydigan modda bo’lgani uchun, SO3 ni dekantatsiyalab ortiqcha qismi olib tashlanadi. S2O3 nam ta’sirida to’q ko’k eritma hosil qiladi.H2SO4 bug’lari ta’sirida jigar rangli kolloid eritma hosil qiladi.
- S2O7-oltingugurt (VII)- oksid SO2 va O2 aralashmasi yog’simon tomchisiga elekrt zaryad ta’sir ettirib Bertlo olgan. 4SO2+3O2=2S2O7
SO2 yoki SO3 ga O3 ta’sir ettirib ham olinadi ammo bu tez parchalanib ketadi.
6SO3+O3=3S2O7
2SO2+O3=S2O7
- SO4-oltingugurt (IV)-oksid. Toza holatda birinchi marta Shvars 1934 yilda olingan.SO2 va O2 aralashmasiga 0,5 mm simob ustuniga teng bosimda elektr zaryad ta’sir ettirib olgan.Qattiq oq modda +3 C da parchalib suyuqlanadi.Suvsiz H2SO4 da parchalanmasdan suyuqlanadi.
SO4’’+[F] = SO4+F2
- Oltingugurt qadim zamonlardan beri ma’lum bo’lgan moddadir. Taxminlarga ko’ra, bu nom Italiyaning ba’zi joylarida gaplashadigan Oskan tilidan lotin tiliga o’tgan. Fors kelib chiqishi deb da’vo qilingan oltingugurt lotin tilidan tarjimada «yonayotgan tosh» degan ma’noni anglatadi. Qadim zamonlardan beri sirli va maftunkor moddalar sifatida qaralgan oltingugurt, ba’zi alkimyogarlar tomonidan moddalarni oltinga aylantirishi kerak bo’lgan » falsafiy tosh » deb ta’riflangan.
- Misrda oltingugurt diniy marosimlarda yoqib yuborilgan. Ushbu sana taxminan 4000 yil oldin qaytib keladi. Injilda oltingugurt «do’zax olovi» deb nomlangan. Qadimgi mualliflardan biri Gomer «Odisseya» da oltingugurt insektitsid sifatida va xonalarning havosini tozalash uchun ishlatilganligini eslatib o’tgan. O’rta asrlarda urushlarda ishlatilgan olov oltingugurt bilan tayyorlangan.




